
P. BOUCHER ET F. BAUDIN LAURENCIN
CNEVA Brest - Laboratoire
de pathologie des animaux aquatiques
BP 70 - 29280 PLOUZANE
Article paru dans "la pisciculture
française", revue de la Fédération Française
d'Aquaculture N° 122; pp. 2-10 (1996).
1 - introduction
En 1976, une nouvelle pathologie
est observée dans les élevages marins de saumon en Ecosse:
la "Maladie du Pancréas" (MP) qui se caractérise par une
destruction totale et spécifique du pancréas exocrine des
smolts passés en mer (Munro et al., 1984). Cette maladie est restée
pendant près de 20 ans sans origine déterminée et
a fait l'objet de controverses: en fait, l'agent responsable de la maladie
est un virus et les lésions caractéristiques de la pathologie
sont non seulement pancréatiques mais aussi musculaires (Nelson
et al., 1995).
Parallèlement, depuis les
années 1980, une nouvelle maladie est observée dans les élevages
bretons de truite arc-en-ciel en eau douce: elle se caractérise
par un comportement particulier des poissons qui se couchent sur le flanc,
au fond des bassins (Figure 1).

Figure 1: truitelles de 5 g présentant
les signes caractéristiques de la MS.
Ce comportement insolite est à l'origine du nom de la pathologie: "Maladie du Sommeil" (MS). Cette MS n'a rien à voir avec la maladie du même nom observée chez l'homme et due à un parasite. Dans un premier temps attribuée à une pollution par les pesticides, c'est récemment qu'une origine virale a été mise en évidence. Les lésions liées à cette maladie sont essentiellement musculaires (Figures 2 et 3) et sont à l'origine du comportement (Boucher et Baudin Laurencin, 1994).

Figure 2: Coupe histologique de muscle
de poisson normal. Le prélèvement est effectué sous
la peau (en haut) au niveau de la ligne latérale dont on voit la
chaîne nerveuse (N). A ce niveau le muscle rouge (R), coupé
transversalement, forme un triangle, bordé par les fibres musculaires
blanches (B).
Coloration hématoxyline -
éosine
Echelle 1cm = 0.3 mm
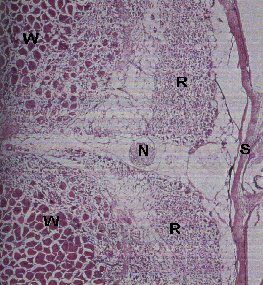
Figure 3: même prélèvement
que précédemment, mais chez un poisson présentant
les signes cliniques de la MS. La peau (en haut) et la chaîne nerveuse
(N) ne sont pas affectées. Les fibres musculaires rouges (R) sont
nécrosées, le muscle profond (B) n'est pas atteint mais on
observe une dégénérescence à la périphérie
du muscle rouge uniquement (muscle intermédiaire).
Coloration hématoxyline -
éosine
Echelle 1cm = 0.3 mm
Les lésions qu'entraînent
cette maladie et la découverte de son caractère infectieux
rapprochent la MS de la "Maladie du Pancréas" (MP). Cet article
décrit comment il a été possible grâce à
l'expérimentation de rapprocher MP et MS, deux maladies qui, a priori,
étaient sans rapport car affectant des espèces différentes,
dans des environnements différents et avec des symptomes et des
lésions distincts.
2 - les études expérimentales: vers une seconde définition de la maladie
L'étude de la "Maladie du Pancréas" (MP) en Bretagne a montré que le saumon élevé en mer présentait des lésions pancréatiques importantes, comme celles observées en Ecosse ou en Irlande (Figure 4).

Figure 4: le pancréas exocrine
est totalement remplacé par des cellules inflammatoires (I). Le
système vasculaire (V) reste présent.
Coloration hématoxyline -
éosine
1 cm = 0.03 mm
L'observation sur le terrain a également
montré que le saumon n'était pas la seule espèce sensible:
les grosses truites fario élevées en mer l'étaient
également. Curieusement, chez les truites fario atteintes de MP,
les lésions pancréatiques sont différentes de celles
observées chez le saumon: les lésions sont nécrotiques
(Figure 5).

Figure 5: nécrose pancréatique
focale. Le pancréas exocrine, qui sécrète les enzymes
digestives, est dans certaines zones apparemment sain et dans d'autres
il est nécrosé.
Coloration hématoxyline -
éosine
1 cm = 0.03 mm
La contamination expérimentale de saumons avec le matériel infectieux "MP" isolé chez la truite fario donne les lésions caractéristiques de la MP telle qu'on l'observe habituellement chez les saumons. Cette constatation suggère que les différences histologiques entre ces deux espèces proviennent d'une différence de sensibilité inter-espèce (Boucher et al., 1995). Partant de cette observation, des essais sont tentés sur une troisième espèce: la truite arc-en-ciel. Chez ce poisson, la MP se déclare également avec des lésions pancréatiques voisines de celles observées chez la truite fario. Parallèlement, au cours des différents essais, des lésions cardiaques et musculaires sont mises en évidence. C'est suite à ces résultats qu'une expérimentation orientée vers la "Maladie du Sommeil" (MS) a été envisagée.
2.1 - présence de lésions pancréatiques; histopathologie séquentielle
A l'origine, la MS se caractérisait
histologiquement par la présence de lésions musculaires uniquement.
Il était intéressant, pour la rapprocher de la MP de vérifier
si elle pouvait également être responsable de lésions
pancréatiques voisines de celles observées chez la truite
arc-en-ciel lors des transmissions expérimentales de la MP.
La maladie se transmet par des broyats
d'organes hématopoïétiques (le rein antérieur
et la rate) ou par le sang de poisson malade. La matière infectieuse
peut être passée sur des filtres de porosité faible
(qui ne laissent passer que les virus) sans perte de virulence. Des essais
de transmission sont effectués sur différentes espèces
de salmonidés d'élevage, comme ceci avait été
fait dans le cas de la MP (Boucher et al., 1995).
2.1.1 - chez la truite arc-en-ciel
L'injection de broyats dilués
de reins antérieurs de poissons malades permet de transmettre la
MS. Dans de l'eau à 13°C, les premières lésions
apparaissent 5 jours après l'injection; ce sont des nécroses
disséminées en foyers du pancréas exocrine. Deux semaines
après injection, les nécroses sont nettement moins fréquentes
et une réaction inflammatoire se développe dans le tissu.
C'est durant cette même période qu'apparaissent les lésions
cardiaques et musculaires. Les lésions cardiaques régressent
après la troisième semaine tandis que l'étendue des
lésions musculaires augmente et culmine généralement
à la troisième ou quatrième semaine après injection.
A cette période, les lésions pancréatiques et cardiaques
ont disparu. Les lésions musculaires disparaissent plus tard, en
moyenne 6 semaines après injection.
Au total, on peut distinguer:
- un stade précoce qui correspond
à la nécrose du pancréas exocrine. A ce stade, les
poissons réduisent significativement la prise alimentaire mais le
stade est trop éphémère pour que l'on observe de réels
problèmes alimentaires;
- un stade intermédiaire qui correspond
à l'inflammation du tissu pancréatique et qui s'accompagne
de lésions myocardiques focales (Figure 6) et épicardiques.
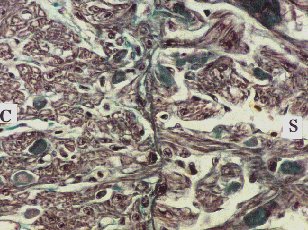
Figure 6: dégénérescence
focale du muscle cardiaque dans les zones compacte (C) et spongieuse (S)
du ventricule. Les fibres musculaires saines sont striées et colorées
en rouge, les fibres en dégénérescence sont colorées
en vert.
Coloration trichrome de Masson
1cm = 0.03 mm
Ces lésions cardiaques pourraient
être responsables d'une plus grande fragilité au stress des
lots malades en élevage: une manipulation du lot malade à
cette période s'accompagne parfois de mortalité soudaine
qui pourrait être attribuée aux lésions cardiaques;
- un stade aigu qui se caractérise
par la disparition quasi complète du muscle superficiel. C'est durant
cette période qu'apparaissent les signes comportementaux de la MS;
- une guérison par régénération
du muscle et du pancréas. Une pancréatite chronique peut
être observée chez certains individus: ces poissons s'amaigrissent
progressivement sans espoir de retour.
Bien que l'ensemble du tableau lésionnel
soit reconstitué expérimentalement, les poissons malades
ne se couchent pas et il n'est donc pas possible de transmettre les signes
cliniques. Pourtant, les lésions musculaires observées sont
importantes et parfois plus étendues que chez certains "poissons
couchés" de pisciculture. La meilleure explication de l'absence
de signe clinique provient des conditions expérimentales: dans les
installations du CNEVA Brest, le courant d'eau est faible ou inexistant;
en pisciculture, au contraire, le courant oblige le poisson à nager
autant qu'il en a la capicité. Quand le muscle rouge encore présent
n'est plus capable d'assurer l'équilibre, le poisson se couche dans
une zone de courant faible. Le syndrome comportemental semble donc lié
à la combinaison d'au moins deux facteurs: les lésions musculaires
et l'environnement de l'animal.
Les lésions musculaires sont
des conditions nécessaires mais pas suffisantes pour expliquer le
comportement du poisson. Ceci justifie également pourquoi, en pisciculture,
certains lots de truites présentent les lésions histologiques
de la MS sans avoir les signes cliniques qui caractérisent la maladie.
L'observation de poissons "asymptomatiques" laisse penser que le nombre
d'épisodes pathologiques de la MS est plus important que les cas
rapportés sur le terrain.
Ces observations mettent en évidence
le manque de connaissance sur les paramètres qui modulent l'importance
de la maladie: les conditions environnementales (température, qualité
du milieu et / ou de l'alimentation, ...), les différences entre
les lots de poissons (souche plus ou moins résistante à la
maladie) et enfin les différences au sein d'un lot (résistance
ou sensibilité individuelles).
2.1.2 - chez la truite fario
La truite fario est, expérimentalement,
peu sensible à la MS... du moins la souche de truite fario testée.
Les lésions pancréatiques sont les seules observées
et elles sont dans tous les cas localisées et ne durent que quelques
jours. Cela explique que la MS "clinique" n'a pu jusqu'ici être observée
dans les élevages.
2.1.3 - chez le saumon atlantique
Chez cette espèce, les lésions
pancréatiques sont très importantes. La plupart du temps,
le pancréas exocrine disparaît totalement en cas de transmission
expérimentale de la MS. Le pancréas exocrine est remplacé
par un tissu fibreux de substitution. Tout le temps où se manifestent
ces lésions (un mois environ), la fonction digestive est inhibée.
Le tissu musculaire (cardiaque et squelettique) n'est que très rarement
lésé.
Les lésions pancréatiques
caractéristiques de la MS peuvent également être transmises
au saumon atlantique si des truites arc-en-ciel ayant la MS sont placées
en aval. La pathologie se transmet donc facilement par l'eau douce (contamination
de 100 saumons par 20 truites arc-en-ciel en une semaine). La cohabitation
de smolts de saumons malades en mer avec d'autres saumons transmet également
la MS: l'agent infectieux peut aussi être véhiculé
par l'eau de mer.
2.1.4 - chez le bar et le turbot
Seules des lésions focales
(nécrose du pancréas) sont observées chez ces espèces.
Elles sont observées seulement une semaine après injection
et disparaissent rapidement. Si ces lésions sont suffisamment marquées
pour constater une sensibilité de ces espèces à la
pathologie, elles sont minimes et le comportement de l'animal n'apparaît
pas affecté.
2.2 - vers une identification de l'agent infectieux
2.2.1 - détermination des caractéristiques
physico-chimiques de l'agent infectieux
Après le succès des
transmissions expérimentales, un matériel infectieux (du
broyat de rein de poisson malade) était disponible. Les tests menés
sur ce matériel infectieux ont permis de remarquer qu'il possédait
des propriétés qui caractérisent les virus enveloppés:
- l'infectiosité est conservée
après passage sur filtre de petite porosité (0.05 microns),
ce qui exclue l'hypothèse d'une origine parasitaire ou bactérienne;
- le matériel virulent reste efficace
après congélation ou lyophilisation;
- la virulence disparaît après
un traitement par la chaleur (60°C pendant 10 minutes) ou un solvant
des lipides (chloroforme).
Ces caractéristiques situent
l'agent infectieux dans la catégorie des petits virus enveloppés
qui comprend deux familles: les togaviridés ("virus à ARN")
et les hépadnaviridés ("virus à ADN").
La famille des hépadnaviridés
regroupe plusieurs virus responsables d'hépatites humaines ou animales.
Bien que ces hépatites soient observées chez de nombreuses
espèces; elles ne sont pas décrites pour l'instant en milieu
aquatique.
Les togaviridés sont, en
revanche, décrits en milieu aquatique chez les crevettes et même
chez le turbot. De plus, dans le cas de la "Maladie du Pancréas"
(MP), des présomptions portent sur un togavirus. Cette caractéristique
est un indice supplémentaire en faveur de la parenté entre
MP et MS.
2.2.2 - observation de particules virales
La recherche de particules virales
dans le matériel infectieux a été longue et difficile:
le virus est présent en faible quantité et au milieu de nombreux
débris cellulaires qui gênent l'observation.
Il a néanmoins été
possible d'observer des particules virales à partir de broyat de
reins de truites atteintes de MS: ces particules mesurent environ 0.045
microns et sont enveloppées (Figure 7), ce qui correspond aux caractéristiques
morphologiques du bioagresseur recherché.

Figure 7: particule virale enveloppée
de la Maladie du Sommeil.
Coloration acide phosphotungstique
1 cm = 0.03 micromètres (0.000
03 mm)
2.3 - épidémiologie, signes cliniques
2.3.1 - répartition géographique,
espèces sensibles, taille, température
La MS est largement observée
en France, essentiellement en Bretagne mais aussi en Aquitaine; en fait
dans les grandes régions d'élevage de truite arc-en-ciel
en eau douce. Des cas très similaires sont rapportés en Espagne
et en Belgique avec les signes cliniques caractéristiques associés
à la dégénérescence musculaire (myopathie)
classiquement observée dans cette pathologie. En Italie, des cas
similaires pourraient être attribués à cette même
pathologie. En Irlande, des myopathies sont également observées:
elles semblent liées à des carences en vitamine E et / ou
sélénium mais la possibilité que l'agent de la MS
puisse intervenir dans le processus pathogène n'est pas exclu.
D'une manière très
générale, c'est chez la truite arc-en-ciel que la maladie
est le plus fréquemment observée. Ceci peut venir d'une plus
grande sensibilité de l'espèce à cette maladie mais
aussi du grand nombre d'élevages de truites arc-en-ciel en eau douce
(car les symptomes de la MS ne sont observés qu'en eau douce). Des
cas typiques sont également observés chez des saumons coho
(avec signes cliniques et lésions caractéristiques) indiquant
clairement que cette espèce est également sensible à
la maladie. Chez des ombles de fontaine et des corégones, des cas
sont aussi rapportés mais la rareté des observations ne permet
pas d'affirmer avec certitude que les symptomes entrevus peuvent être
rapportés à la MS. Expérimentalement, des lésions
caractéristiques ont été transmises aux truites arc-en-ciel
et fario, au saumon atlantique (parr en eau douce et smolt en mer) ainsi
que chez des bars et des turbots.
La MS affecte les poissons quelles
que soient leurs tailles (de 1 g à 1 kg ou plus...) ou la saison
(et donc la température de l'eau). Le plus souvent, cependant, la
maladie est présente au printemps, chez des truitelles de 10 à
50 g, dans des eaux dont la température varie de 9 à 13°C.
2.3.2 - signes cliniques, explication
du comportement
La MS est caractérisée
par un comportement très particulier du poisson qui ne parvient
plus à maintenir sa posture naturelle. Le poisson malade se couche
sur le fond du bassin, dans une zone de faible courant; il est capable
de reprendre une nage rapide de fuite s'il se sent menacé (par une
épuisette par exemple) mais cette nage s'effectue généralement
sur le côté ou en vrille et le poisson se recouche quelques
mètres plus loin (Figure 1). D'autres poissons sont en surface,
également sur le flanc, comme des poissons morts; ces individus
sont plus faciles à capturer à l'épuisette et ce sont
les seuls individus malades que l'on observe lorsque l'eau est boueuse.
Il est également possible de capturer des individus malades sur
les grilles d'évacuation des bacs où ils sont plaqués
par le courant. Les poissons prélevés à ce niveau
sont souvent marqués par la grille, témoignant d'une longue
période d'immobilité.
Habituellement, le pourcentage de
poissons couchés dans un lot atteint est d'environ 10% (±
5%). Plus rarement, ce taux peut atteindre jusque 50% de l'effectif. Il
n'est pas possible d'affirmer si ce sont toujours les mêmes poissons
que l'on observe couchés ou si une partie des individus se couche
pendant un certain temps puis est relayé par d'autres poissons malades.
Le "syndrome du poisson couché"
a pendant longtemps été attribué à une pollution
par les pesticides. En effet, un épisode de MS avait été
rapporté en aval d'une cressonnière traitée par des
pesticides (carbamates). De plus, le comportement du poisson était
similaire à celui d'un animal intoxiqué par les pesticides:
ces produits, généralement constitués d'inhibiteurs
de l'acétylcholine estérase, bloquent la transmission d'information
entre le système nerveux et musculaire, ce qui entraîne une
paralysie musculaire (souvent responsable de la mort lorsque les muscles
vitaux sont touchés). Une telle paralysie aurait, par conséquent,
pu être responsable du comportement du poisson. Les nombreux essais
expérimentaux effectués en laboratoire avec plusieurs pesticides
couramment utilisés en agriculture n'ont cependant jamais permis
de transmettre les signes cliniques de la MS: le poisson en fonction des
doses meurt ou survit. S'il reste possible que des pollutions puissent
favoriser des signes comportementaux proches de ceux de la MS, la maladie,
telle qu'elle est actuellement définie suit un développement
séquentiel bien établi et distinct.
En fait, il est maintenant évident
que le comportement du poisson est lié aux lésions musculaires,
le système nerveux ne semblant pas affecté. Le muscle rouge
superficiel, qui peut être totalement détruit dans les cas
extrêmes, est responsable de la nage de maintien du poisson. Sa destruction
suffit à expliquer la perte d'équilibre du poisson (Figures
2 et 3). Le muscle blanc, qui est moins altéré par la pathologie
est responsable de la nage rapide induite par le stress dans la réaction
de fuite. Le poisson est donc incapable de maintenir sa posture normal
du fait de ses lésions du muscle rouge mais reste par contre capable
de fuir lorsqu'il se sent menacé grâce au muscle blanc encore
fonctionnel.
Les études menées
au CNEVA Brest ont cependant montré que les lésions musculaires
apparaissent dans une phase ultime de la maladie, qui est précédée
systématiquement par des lésions pancréatiques. De
la même façon, sur le terrain, on a pu observer que des lésions
musculaires étaient précédées de lésions
pancréatiques identiques à celles décrites expérimentalement
(Figures 4 et 5) mais jusqu'ici négligées.
2.3.4 - impact de la maladie sur l'élevage
D'une manière générale,
la MS est responsable de faible mortalité (de l'ordre de 5%). Cependant,
Il est parfois fait état de mortalité de 10 à 15%,
voire 40%. Cette mortalité pourrait être imputable à
des pathologies intercurrentes: les poissons qui se couchent au fond ne
s'alimentent plus et s'affaiblissent. De plus, ils se frottent au fond
des bassins et fragilisent ainsi leur barrière cutanée. La
pénétration de germes opportunistes, généralement
des bactéries, n'est donc pas surprenante dans ce contexte; ces
pathologies secondaires peuvent être responsables de mortalités
importantes et brutales se déroulant sur une courte période.
Les infections bactériennes
opportunistes ne sont cependant pas systématiquement mises en évidence
même lorsque la mortalité est élevée, ce qui
suggère que certaines populations de truites arc-en-ciel pourraient
montrer une sensibilité particulière à la MS et présenter
une mortalité significative même en l'absence d'infections
secondaires.
L'épisode infectieux dure
environ 2 mois durant lesquels le poisson malade s'alimente peu. Cette
baisse de l'appétit est lié aux lésions pancréatiques
causées par la maladie: le pancréas exocrine, impliqué
dans les synthèses d'enzymes digestives est partiellement détruit
et l'aliment est difficilement assimilé. Un amaigrissement du poisson
peut s'ensuivre et, plus grave encore, le développement de pancréatites
chroniques empêchant la croissance des poissons qui atteignent difficilement
la taille adulte ou qui restent trop maigre pour être commercialisés.
La MS a donc deux conséquences
pour l'éleveur: d'une part une mortalité à court terme
(durant le développement de la maladie) et d'autre part, à
long terme, une croissance difficile pour certains lots, séquelle
de l'épisode pathologique.
2.4 - nouvelle définition de la Maladie du Sommeil
La MS apparaît aujourd'hui comme une maladie virale, infectieuse et contagieuse, touchant plusieurs espèces de salmonidés et se traduisant par la succession chronologique de lésions dégénératives d'abord pancréatiques puis cardiaques et musculaires (principalement le muscle rouge superficiel). Les symptomes comportementaux sont la conséquence, dans un environnement particulier, de la dégénérescence intense du muscle rouge superficiel.
3 - la Maladie du Sommeil: une ressemblance
avec la Maladie du Pancréas
3.1 - similarité lésionnelle des pathologies
La MP n'est pas responsable que de
lésions pancréatiques, comme l'ont suggéré
les laboratoires écossais pendant 15 ans. La "Maladie du Pancréas"
(MP) est souvent associée à d'autres pathologies: le "Syndrome
de la Cardiomyopathie" (SCM), pouvant conduire au "Syndrome de la Mort
Soudaine" (SMS), et la "myopathie squelettique aiguë" (MSA). Dans
certaines conditions ou sur certaines populations de saumons, la MP peut
être responsable de lésions cardiaques (SCM) et musculaires
(MSA), ce qui la rapproche de la MS. Les lésions rencontrées
en cas de MSA sont les mêmes que celles observées en cas de
MS: une dégénérescence des fibres musculaires qui
touche prioritairement le muscle rouge. De même, en cas de MS, les
lésions cardiaques observées sont du même type que
celles décrites en cas de SCM avec une moins grande importance.
Les lésions pancréatiques sont aussi moins importantes en
cas de MS que de MP.
MP et MS sont deux pathologies responsables
de lésions pancréatiques, cardiaques et musculaires; le type
de lésion est identique entre les deux maladies mais l'étendue
de ces lésions diffère. La MP est une pathologie du saumon
atlantique en mer et la MS une pathologie de la truite arc-en-ciel en eau
douce: ces différences entre espèces et entre milieux pourraient
être responsable des variations d'importance des lésions.
Enfin, il convient de rappeler que
si la MS est observée sur les principales zones de production de
truite arc-en-ciel, la MP est étendue aux zones de production de
saumon (Ecosse, Irlande, France, Espagne, Norvège, Etats Unis et
Canada).
3.2 - similarité morphologique des virus responsables
L'isolement récent d'un virion appelé "Virus de la Maladie du Pancréas du Saumon" (VMPS) par les chercheurs irlandais fait état d'un petit virus enveloppé à ARN, probablement un togavirus (Nelson et al., 1995). L'aspect du virus est identique à celui observé sur des truites arc-en-ciel atteintes de MS. Les données sont encore trop imprécises pour que l'on puisse établir une parenté entre ces deux particules virales. Le fait que ces particules puissent être de la même famille est néanmoins un facteur supplémentaire en faveur d'une parenté entre MP et MS.
3.3 - Maladie du Pancréas et Maladie du Sommeil: deux pathologies aux agents difficiles à isoler
La difficulté d'identification
de l'agent responsable des pathologies constitue un autre point commun
entre MP et MS. Il aura fallu en effet pour chaque maladie plus de 15 ans
de recherche pour obtenir les premières observations du bioagresseur.
Le ou les agents infectieux responsable(s) de ces pathologies sont donc
plus difficiles à caractériser par les méthodes classiques
de diagnostic que les maladies habituellement rencontrées en élevage
piscicole. Cette constatation peut être le fruit d'une simple coïncidence
ou, au contraire, un indice supplémentaire de parenté.
Nous sommes en effet aux premières
avancées notables dans la compréhension de la MP comme de
la MS; si les agents infectieux sont du même type, leurs moyens d'identification
seront les mêmes. Quelques résultats encourageants ont par
exemple été obtenus en culture cellulaire dans le cas de
la MP; nous tentons actuellement de le appliquer à la MS.
3.4 - protection croisée entre Maladie du Pancréas et Maladie du Sommeil
Les recherches menées en Ecosse
sur la MP ont permis de démontrer une protection acquise vis à
vis de la maladie: des saumons ayant eu un premier épisode pathologique
de MP sont immunisés et ne font pas la maladie une deuxième
fois. Cette protection dure au moins 9 mois (durée de l'expérience)
et persiste même après le transfert en mer (Houghton, 1994).
L'immunité acquise vis à
vis de la MP existe également chez la truite arc-en-ciel. Partant
du principe que MP et MS sont des maladies voisines, nous avons démontré
que la MS déclenche un mécanisme immunitaire de protection
acquise. Plus intéressant encore: une truite ayant eu un premier
épisode infectieux de MP ou de MS est immunisée contre les
deux pathologies. Cette protection croisée entre MP et MS est un
argument important en faveur d'une parenté entre les deux maladies
(Boucher, 1995). En effet, cette observation indique que l'antigénicité
de la MP est très voisine de la MS: le système immunitaire
ne distingue pas les deux agents infectieux, ce qui suggère qu'ils
sont similaires. Bien évidemment, ceci ne constitue pas une démonstration
que les agents de la MP et de la MS sont similaires, voire identiques,
car il existe des cas de maladies aux bioagresseurs différents qui
génèrent des protections croisées. Cependant, ces
exemples sont rares et la protection croisée entre les deux maladies
n'est qu'un argument supplémentaire à ajouter aux précédents
et qui sont tous en faveur d'une similarité MP/MS.
Si la protection croisée
entre les deux maladies apporte un résultat fondamental intéressant;
au niveau pratique, cette donnée est également très
utile. Des truites qui ont développé un épisode de
MS en eau douce pourraient être résistantes à des épisodes
de MP en mer. Il est moins dommageable pour un pisciculteur de perdre des
petits poissons que des gros et des truitelles qui ont bien récupérées
de la MS seraient des poissons plus résistants à la MP comme
la MS par la suite (?).
4 - méthodes de diagnostic
Outre les signes comportementaux
qui la caractérisent, la MS est responsable, comme indiqué
précédemment, de lésions histologiques importantes
qui servent au diagnostic de la maladie. En fait, les symptomes n'apparaissent
que lorsque les lésions sont très prononcées et dans
certaines conditions. La maladie peut donc exister sans apparition des
symptomes, c'est l'observation des lésions qui permet alors de faire
le diagnostic.
Les organes lésés
libèrent cependant dans la circulation générale des
enzymes qui peuvent être dosées, permettant un suivi plus
facile des élevages. Dans l'impossibilité d'une mise en évidence
directe de l'agent causal, ces deux méthodes restent les seules
actuellement utilisables.
4.1 - diagnostic par histologie
Le critère le plus significatif
est sans aucun doute la disparition partielle ou totale des fibres musculaires
rouges. Le prélèvement doit s'effectuer préférablement
de part et d'autre de la ligne latérale, à mi-longueur de
l'animal (sous la nageoire dorsale), car c'est à ce niveau que le
muscle rouge est le plus épais (Figures 2 et 3). Pour une bonne
pénétration du fixateur (liquide de Bouin de préférence),
l'échantillon doit être de petit volume (3 à 4 mm d'épaisseur
pour une longueur de 1 à 2 cm, cette plus grande dimension étant
perpendiculaire à la ligne latérale). Dans ces conditions,
les faisceaux de fibres musculaires seront coupés transversalement
pour permettre d'estimer sommairement le pourcentage de perte musculaire.
Le tissu restant est constitué de fibres musculaires "normales"
ou en voie de dégénérescence; ainsi que de cellules
du sarcolemme (qui participent à la régénération
du tissu détruit) et de cellules inflammatoires. Le muscle blanc
également prélevé est dans tous les cas moins atteint
que le muscle rouge même si parfois plusieurs fibres sont touchées.
Il n'existe pas de relation directe
entre le degré des lésions musculaires et les symptomes.
Tous les poissons couchés montrent systématiquement des lésions
importantes du muscle rouge. En revanche, parmi les poissons prélevés
"apparemment sains" (nage normale, bonne prise alimentaire), un certain
pourcentage de poisson présentent des lésions musculaires...
dont certaines sont encore plus marquées que celles observées
sur les "poissons couchés"! Par ailleurs, si le comportement anormal
du poisson suppose des lésions musculaires prononcées, l'existence
des mêmes lésions n'entraîne pas systématiquement
le dit comportement.
S'il est clair que dans un lot affecté,
tous les individus développent les lésions caractéristiques
de la maladie (vu son degré de contagiosité), en revanche
l'existence de porteurs asymptomatiques complique le problème car
certains lots de poissons peuvent être touchés par la maladie
sans aucun signe apparent (car la population est plus résistante?).
Le risque à ce moment de déplacer des poissons malades sans
le savoir et ainsi de contaminer d'autres individus plus sensibles existe.
Outre les lésions du muscle
squelettique, des lésions du muscle cardiaque sont fréquemment
observées. Ces lésions qui se traduisent par une perte de
fibres sont dans tous les cas focales et ne semblent pas affecter le poisson
(Figure 6). Il reste néanmoins que le coeur est un organe vital,
ce qui pourrait expliquer des mortalités soudaines de poissons suite
à des interventions stressantes (manipulation).
Dans l'état actuel de nos
connaissances, et en l'absence de corrélation entre l'étendue
des lésions cardiaques et le pourcentage de mortalité, rien
ne nous permet d'affirmer que les lésions cardiaques soient impliquées
dans les mortalités.
Le pancréas exocrine est
également affecté par la maladie. Ce tissu, impliqué
dans la sécrétion d'enzymes digestives, est parfois partiellement
détruit par une nécrose (Figure 5) chez des individus qui
par ailleurs sont apparemment sains et ne présentent pas de lésions
musculaires. Une réaction inflammatoire peut aussi être observée;
chez certains individus, elle peut envahir tout le pancréas exocrine
qui dans ce cas disparaît complètement (Figure 4). De tels
poissons ont généralement des lésions musculaires
importantes. Enfin, il peut exister des poissons à lésions
musculaires importantes et avec un pancréas exocrine histologiquement
normal.
4.2 - diagnostic par dosage enzymatique
Si l'observation histologique du
muscle rouge reste le seul et unique moyen de diagnostiquer avec certitude
la MS, le dosage sanguin des enzymes d'origine musculaire peut orienter
le diagnostic. La dégénérescence de fibres musculaires
libère en effet dans le plasma des quantités importantes
de Créatine Kinase (CK), alanine amino-transférase (ALAT)
et aspartate amino-transférase (ASAT). Parmi ces trois enzymes,
la montée du taux de CK est la plus significative puisqu'elle peut
atteindre 70 fois les taux habituellement observés (pour ALAT et
ASAT, l'augmentation peut approcher 40 fois les taux normaux). Le prélèvement
sanguin peut s'effectuer dans la veine caudale même s'il faut traverser
un tissu musculaire: l'augmentation des CK lié à la prise
de sang est insignifiante par rapport à ce que l'on observe en cas
de myopathie aiguë comme c'est le cas de la MS. Il est préférable
néanmoins, pour les gros individus, d'effectuer la prise de sang
dans le canal de Cuvier. Une truite qui présente des taux de GPT,
GOT et CK respectivement supérieurs à 300, 5000 et 10 000
UI a probablement des lésions musculaires.
Dans le cas où le pancréas
est fortement détruit par la maladie, il en résulte une hypofonction
de cette organe qui se traduit par une baisse sensible du taux sanguin
d'amylase pancréatique: généralement, une amylasémie
faible (inférieure à 500 UI) correspond à un pancréas
en dessous de ses capacités normales.
La maladie entraîne un affaiblissement
général du poisson, ce qui a des répercussions indirectes
sur d'autres paramètres sériques: le taux de protéines
totales diminue, comme la cholestérolémie. Des déséquilibres
osmotiques peuvent aussi être observés.
L'intérêt principal
du dosage enzymatique est qu'il permet d'apprécier l'importance
de la maladie dans une pisciculture, en ne tenant pas seulement compte
des poissons présentant les anomalies du comportement. Les activités
enzymatiques, plus faciles à rechercher sur un grand nombre que
les lésions histologiques, permettent le suivi de la maladie dans
l'ensemble de l'élevage: nombre de lots affectés, gravité
de la maladie dans chaque lot, phase évolutive,...
Le dosage enzymatique a néanmoins
ses limites: d'autres maladies que la MS provoquent des lésions
musculaires et par conséquent une augmentation des enzymes musculaires.
Les indications apportées ne sont donc à considérer
que dans le contexte de MS identifiée par histologie.
5 - la Maladie du Sommeil: perspectives
de recherche
La mise en culture cellulaire du
virus responsable de la MS reste une priorité qui permettra non
seulement un diagnostic de la maladie mais aussi et surtout de pouvoir
expérimenter plus facilement grâce à une production
virale à un titre déterminé et avec un degré
de pureté suffisant.
Ceci devrait permettre notamment
la production d'anticorps spécifiquement dirigés contre le
virus, ce qui serait utile pour un diagnostic fiable et reproductible de
la maladie. A plus long terme, la production d'un vaccin serait envisageable,
dans la mesure où les pertes générées par la
maladie rendraient rentable cette vaccination.
La MS n'est pas habituellement responsable
de fortes mortalités (généralement 10-15%) mais ces
mortalités peuvent dépasser 40% dans certains cas. Plus grave
que la MS elle-même, le risque de développement au moment
de l'épisode pathologique de maladies opportunistes: les poissons
malades qui sont affaiblis par le manque de nourriture et qui perdent une
partie de leur protection externe en se frottant au fond des bassins sont
exposés à des maladies essentiellement bactériennes
qui déclenchent une forte mortalité sur une courte période.
Le rôle joué par ces maladies opportunistes et l'impact qu'elles
ont sur la mortalité sont actuellement mal établis; des recherches
dans ce domaine pourraient permettre de mieux comprendre le tableau pathologique
et aussi de limiter la mortalité.
De plus, la MS peut chez certains
individus générer des pancréatites chroniques qui
n'entraînent pas de mort mais des retards de croissance conduisant
à des poissons trop maigres pour être commercialisés.
Les lésions pancréatiques dues à la MS sont systématiques,
en revanche l'hypofonction du pancréas exocrine semble être
liée à une réaction inflammatoire excessive. Le problème
économique que peut représenter des individus qui ne récupèrent
jamais totalement de la maladie est suffisamment important pour que l'on
tente de rechercher pourquoi ce phénomène de pancréatite
chronique n'est observé que chez certains poissons.
BOUCHER, P. & BAUDIN LAURENCIN, F.
(1994) Sleeping disease of salmonids. Bull. Eur. Ass. Fish Pathol. Vol
14 (5); pp. 179-180
BOUCHER, P., CASTRIC, J. & BAUDIN
LAURENCIN, F. (1994) Observation of virus-like particles in rainbow trout
Oncorhynchus mykiss infected with Sleeping disease virulent material. Bull.
Eur. Ass. Fish Pathol. Vol 14 (6); pp. 215-216
BOUCHER, P. (1995) Etiologie et pathogénie
de la Maladie du Pancréas et de la Maladie du Sommeil chez les salmonidés
d'élevage. Thèse de l'Université de Rennes I, n°
1402; 254 p.
BOUCHER, P., RAYNARD, R.S., HOUGHTON,
G. & BAUDIN LAURENCIN, F. (1995) Comparative histopathology of pancreas
disease in Atlantic salmon, Rainbow trout and brown trout. Dis. aquat.
Org., Vol 22; pp. 19-24
HOUGHTON, G (1994) Acquired protection
in Atlantic salmon Salmo salar parr and post-smolts against pancreas disease.
Dis. Aquat. Org., Vol 18; pp. 109-118
MUNRO, A.L.S., ELLIS, A.E., Mc VICAR,
A.H., Mc LAY, H.A. & NEEPHAM, E.A. (1984) An exocrine pancreas disease
of farmed Atlantic salmon in Scotland. Helgoländer Meeresunters, Vol
37; pp. 571-586
NELSON, R.T., Mc LOUGHLIN, M.F., ROWLEY,
H.M., PLATTEN, M.A. & Mc CORMICK, J.I. (1995) Isolation of a toga-like
virus from farmed Atlantic salmon Salmo salar with pancreas disease. Dis.
Aquat. Org.; Vol 22; pp. 25-32